Las baterías de litio azufre prometen grandes capacidades energéticas pero tienen su hándicap principal en la rápida degradación que sufren con los ciclos de carga y descarga, lo que se traduce en una escasa vida útil. Un equipo de investigadores de la Universidad de Michigan ha creado una nueva membrana de batería "de inspiración biológica" que permite que una batería de litio-azufre ofrezca una capacidad energética cinco veces superior a las de iones de litio y se mantenga funcionando durante los más de mil ciclos necesarios para alimentar un vehículo eléctrico.
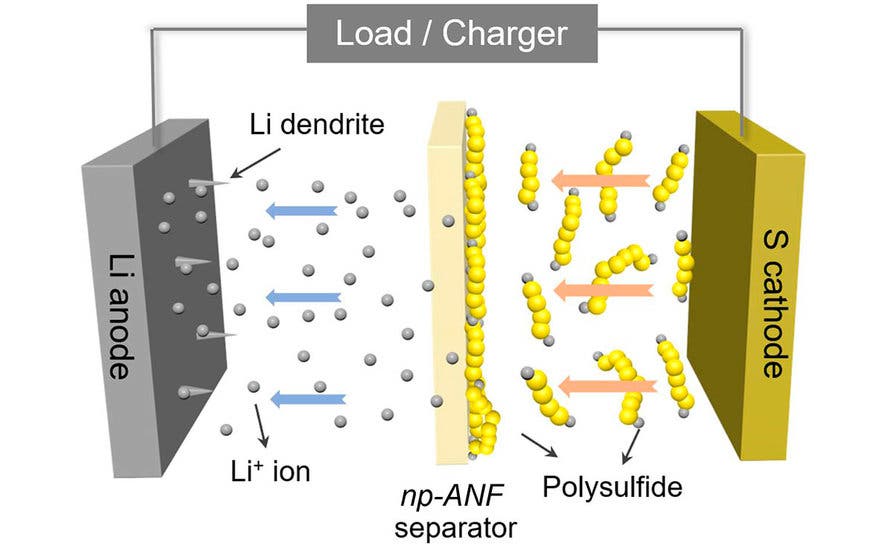
La tecnología de las baterías de Li-S es una de las más prometedoras en la actualidad por sus ventajas técnicas, económicas y medioambientales. En el caso de los vehículos eléctricos, su mayor capacidad energética y su menor coste podrían ayudar a reducir la brecha de precio y de autonomía respecto a los modelos de combustión. Sin embargo, a diferencia de las de iones de litio, la reacción química que se produce en el interior de las baterías de azufre conduce a la acumulación de sulfuro de litio sólido y polisulfuro de litio líquido lo que provoca una pérdida de material activo en el cátodo de azufre (electrodo negativo) y la corrosión del ánodo de litio (electrodo positivo). Esto se traduce directamente en una mayor degradación de la batería y por lo tanto en una vida útil muy limitada.
Para resolver este problema, el equipo de investigadores de la Universidad de Michigan ha demostrado que una membrana nanofibras de aramida, recicladas de Kevlar, permite que las baterías de litio-azufre superen su talón de Aquiles: la degradación.
La vida útil de una batería se mide por la cantidad de ciclos de carga y descarga que es capaz de soportar sin que se aprecie una degradación excesiva en su capacidad energética. En el caso de las baterías de Li-S hay algunas investigaciones que afirman haber logrado varios cientos de ciclos, pero todas ellas a expensas de reducir otros parámetros fundamentales como la capacidad y la potencia de recarga, la resiliencia e incluso la seguridad. El desafío para los investigadores es lograr satisfacer las necesidades de un vehículo eléctrico "cumpliendo con cada uno de estos parámetros e incluyendo el coste", afirma Nicholas Kotov, profesor de ciencias químicas e ingeniería de la Universidad Irving Langmuir, y director de la investigación.
La ingeniería biomimética de estas baterías integró dos escalas: molecular y nanoescala. Anteriormente, el equipo se había basado en redes de nanofibras de aramida infundidas con un gel electrolítico para detener una de las principales causas de los cortos ciclos de vida de estas baterías: las dendritas que crecen de un electrodo al otro, perforando la membrana. La dureza de las fibras de aramida detiene las dendritas. Sin embargo esta estrategia no fue suficiente.
Las baterías de litio- azufre tienen otro problema: las pequeñas moléculas de litio y azufre que se forman y que fluyen hacia el litio, se adhieren y reducen la capacidad de la batería. La membrana necesitaba permitir que los iones de litio fluyeran del litio al azufre y viceversa, bloqueando las partículas de polisulfuros de litio. Esta capacidad se denomina selectividad iónica.
"Nos inspiramos en los canales de iones biológicos y diseñamos carreteras para los iones de litio en los que los polisulfuros de litio no pueden pasar por los peajes", explica Ahmet Emre, investigador postdoctoral en ingeniería química y coautor del artículo publicado en Nature Communications. Los iones de litio y los polisulfuros de litio tienen un tamaño similar, por lo que no era suficiente con bloquear los polisulfuros creando pequeños canales. Los investigadores agregaron una carga eléctrica a los poros de la membrana de la batería aprovechando los propios polisulfuros de litio. Estos se adhirieron a las nanofibras de aramida repeliendo los iones de polisulfuro de litio que continúan formándose en el electrodo de azufre mientras que los iones de litio cargados positivamente pasaban libremente.

Al comienzo del experimento, los polisulfuros de litio están solo en el lado izquierdo de la celda de la batería, tanto para la membrana industrial de la izquierda como para la membrana de nanofibras de aramida de la derecha. Media hora después la membrana industrial filtra los polisulfuros de litio y tras 96 horas la membrana de aramida bloquea completamente los polisulfuros. Imagen Ahmet Emre, Kotov Lab.
Según Kotov, esta batería tiene el diseño "casi perfecto" para cumplir con todos los parámetros que exigen los vehículos eléctricos, incluida la sostenibilidad de su producción. Su capacidad y su eficiencia se acercan a los límites teóricos. Permiten temperaturas extremas, desde las más altas que se producen durante la recarga rápida hasta las más frías e invernales. Con más de 1.000 ciclos de carga y descarga la vida útil de la batería puede llegar a alcanzar los 10 años.
También ofrece ventajas en cuanto a sosteniblidad. El azufre es mucho más abundante que el cobalto de los electrodos de las baterías de los iones de litio y las fibras de aramida para la membrana se pueden reciclar a partir de chalecos antibalas antiguos.
La investigación fue financiada por la Fundación Nacional de Ciencias y el Departamento de Defensa. El equipo estudió la membrana en el Centro de Caracterización de Materiales de Michigan. La Universidad de Michigan ha patentado la membrana y Kotov está poniendo en marcha una empresa para llevarla al mercado.